ອາຊິດ amino ແມ່ນຫຍັງ?
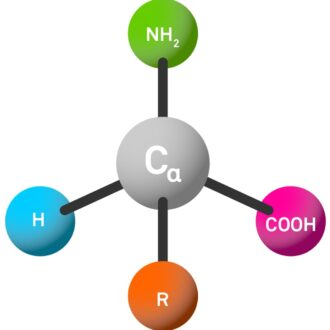
ອາຊິດ amino ທີ່ພົບເລື້ອຍທີ່ສຸດໃນທໍາມະຊາດແມ່ນເອີ້ນວ່າກົດα-amino. ໂມເລກຸນເຫຼົ່ານີ້ມີ 4 ທົດແທນທີ່ແຕກຕ່າງກັນທີ່ຕິດຢູ່ໃນປະລໍາມະນູ Centr DEVEL (ທີ່ເອີ້ນວ່າα-c Atom):
ມິໂນ (NH₂, ລະຫັດສາມຈົດຫມາຍຫຍໍ້ຫຍໍ້ເປັນ "h-").
ກຸ່ມອາຊິດ Carboxylic (COOH, ຫຍໍ້ເປັນ "- -OH" ໃນລະຫັດສາມຈົດຫມາຍ).
ຕ່ອງໂສ້ຂ້າງ(r, ເຊິ່ງມີຄວາມປ່ຽນແປງສູງແລະກໍານົດຄຸນສົມບັດຂອງອາຊິດ amino ເຊັ່ນດຽວກັນກັບ peptide ສຸດທ້າຍ).
ປະລໍາມະນູໄຮໂດຼລິກ (h).
ການເຊື່ອມຕໍ່ຂອງ ATOMs α-c ກັບສີ່ກຸ່ມທີ່ແຕກຕ່າງກັນນີ້ເຮັດໃຫ້ມີຄຸນລັກສະນະທີ່ເປັນເອກະລັກ, ເຊິ່ງມີບົດບາດສໍາຄັນໃນການກໍານົດພຶດຕິກໍາແລະຄຸນສົມບັດຂອງອາຊິດ amino ແລະ peptides.
ກິດຈະກໍາດ້ານຊີວະວິທະຍາຂອງອາຊິດ amino
ອາຊິດ amino ສາມາດສະແດງກິດຈະກໍາດ້ານຊີວະວິທະຍາເຊັ່ນ:
Tryptophan (TRP) ແລະອາຊິດ glutamic (glu) ມີບົດບາດສໍາຄັນໃນຂະບວນການຍ່ອຍອາຫານ.
ກຸ່ມ R (ຫຼືລະບົບຕ່ອງໂສ້ຂ້າງ) ກໍານົດຄຸນສົມບັດທີ່ເປັນເອກະລັກຂອງອາຊິດ amino. ກຸ່ມເຫຼົ່ານີ້ສາມາດ:
ໃນເງື່ອນໄຂທີ່ງ່າຍດາຍ:ປະລໍາມະນູ hydrogen ຄ້າຍຄື glycine (gly).
ອາຊິດອື່ນໆແມ່ນລວມຢູ່: ເຊັ່ນວ່າອາຊິດ aspartic (ASP) ແລະອາຊິດ glutamic (glu).
ປະຕິບັດກຸ່ມພື້ນຖານ:arginine (Arg), lysine (lys) ຫຼື histidine (ລາວ).
ປະກອບມີກຸ່ມຂົ້ວໂລກ: ເຊັ່ນ: Serine (Ser) ຫຼືໄພຂົ່ມຂູ່ (thr).
hydrocarbons ທີ່ບໍ່ແມ່ນເຂດປອດໄພ:Alanine (ALA), Phenylalanine (Phe) ຫຼື valine (val).
ເນື້ອໃນຊູນຟູຣິກ:ດັ່ງທີ່ເຫັນໃນ cystine (cys) ແລະ methionine (ໄດ້ພົບ).
ບົດບາດຂອງ L -Mino ACIDS ແລະ D -MOIN ACIDS
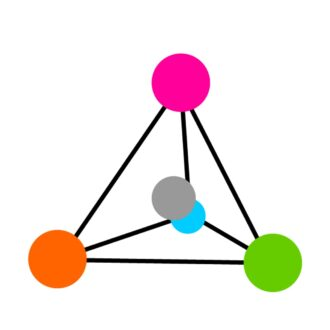
ປະລໍາມະນູ 4 ຄົນຂອງປະລໍາມະນູα-c ແມ່ນຈັດຢູ່ບ່ອນຂອງ tetrahedron, ໂດຍມີα-c Atom ຢູ່ໃນສູນກາງ (ເບິ່ງຮູບທີ 3). ການຈັດການນີ້ອະນຸຍາດໃຫ້ມີສອງຮູບແບບຂອງໂມເລກຸນອາຊິດ amino ທີ່ມີຢູ່ໃນກະຈົກ, ຄ້າຍຄືກັບມືຊ້າຍແລະຂວາ. ຮູບແບບກະຈົກເຫຼົ່ານີ້ແມ່ນເປັນທີ່ຮູ້ຈັກວ່າ "Stereoisomers" ຫຼື "Enantiomers".
ຄວາມສໍາຄັນດ້ານຊີວະວິທະຍາຂອງ Enantiomers
ເຖິງແມ່ນວ່າ Enantiomers ມີຄຸນສົມບັດທາງເຄມີແລະທາງກາຍະພາບເກືອບ, ຜົນກະທົບທາງຊີວະພາບຂອງພວກມັນສາມາດແຕກຕ່າງກັນຢ່າງຫຼວງຫຼາຍ. ຮູບຊົງໂມເລກຸນແມ່ນສໍາຄັນຕໍ່ການພົວພັນກັບເປົ້າຫມາຍທາງຊີວະພາບ. ຫນຶ່ງ enantiomer ອາດຈະຜູກມັດຢ່າງມີປະສິດຕິຜົນຕໍ່ເປົ້າຫມາຍ, ອີກອັນຫນຶ່ງອາດຈະບໍ່, ຫຼືໃນບາງກໍລະນີມີຜົນກະທົບທາງລົບ. ໃນການແກ້ໄຂ, Enantiomer ໄດ້ຫມູນຍົນແສງສະຫວ່າງທີ່ຂົ້ວໂລກໃນທິດທາງກົງກັນຂ້າມ.
ເວລາໄປສະນີ: 2025-09-05
